
相信大家经常看到各种电动车电池起火爆炸的新闻,可是造成这些危险事故的原因是什么呢?今天小编从科学的角度给大家普及一下。
我们知道蓄电池的工作过程,就是电能与化学能转化过程。充电是将电能转化为化学能存到电池里,放电就是把化学能幻化为电能,来驱动用电设备。
一:电势;
要理解蓄电池的工作原理,首先要了解电势的建立过程。电解液是硫酸+水的硫酸水溶液。硫酸在水分子的作用下电离:H2SO4=HSO4-+H+。由于极板上的少量活性物质溶于电解液,就产生了电极电位,正负极板电极电位不同,就形成了电动势。
正极板上的二氧化铅溶于电解液,与水生成氢氧化铅,再离解成正四价铅离子Pb4+和氢氧根离子OH-。现在,正极极板上就有了Pb4+,正极板电位就比电解液高2.0V。
负极板上的活性物质铅Pb,失去电子生成了二价铅离子Pb2+,溶于电解液中,电子留在负极板上,负极板就和电解液建立了电极电位,约为-0.1V.
这样,蓄电池的正负极板就形成了2.1V电位差。蓄电池的一个电池格就是2.1V,6个电池格就组成了一块铅酸电池12V。
为了便于理解,我们更简单明了的介绍充电和放电过程:
二:放电;

放电就是化学能转化为电能的过程。放电时,电流从正极经过用电设备流到负极,也就是电子从负极到正极的过程。极板上的活性物质铅全部变成硫酸铅,电解液的密度慢慢减小,电池内阻不断升高,一直到这个化学反应停止,也就是电用完了。
三:充电;

充电就是把电能转化成化学能的过程。蓄电池接上充电器电源,外部电压高于过蓄电池的电动势时,电流又从负极流向正极,和放电过程时相反的。硫酸铅又慢慢的还原成了放电前的状态——活性物质铅,电解液的密度越来越大,直到不再反应位置。
铅酸电池的安全性:
铅酸电池的这三个过程相对安全,危险无非是过充过放而导致的电池鼓包,因为金属铅是一种耐腐蚀的中有色金属材料。铅的熔点327℃,沸点1740℃。除了对环境有污染,铅是非常安全的。
锂电池的原理:
锂电池的机构基本结构都是相同的,不管磷酸铁锂还是三元锂,都是由正极材料、负极材料、隔膜还有电解液组成。
一:放电;

锂电池放电过程
放电过程是锂离子从负极流向正极的过程,锂离子嵌入到正极。过放的话,锂离子就会堆积在正极板。
二:充电;
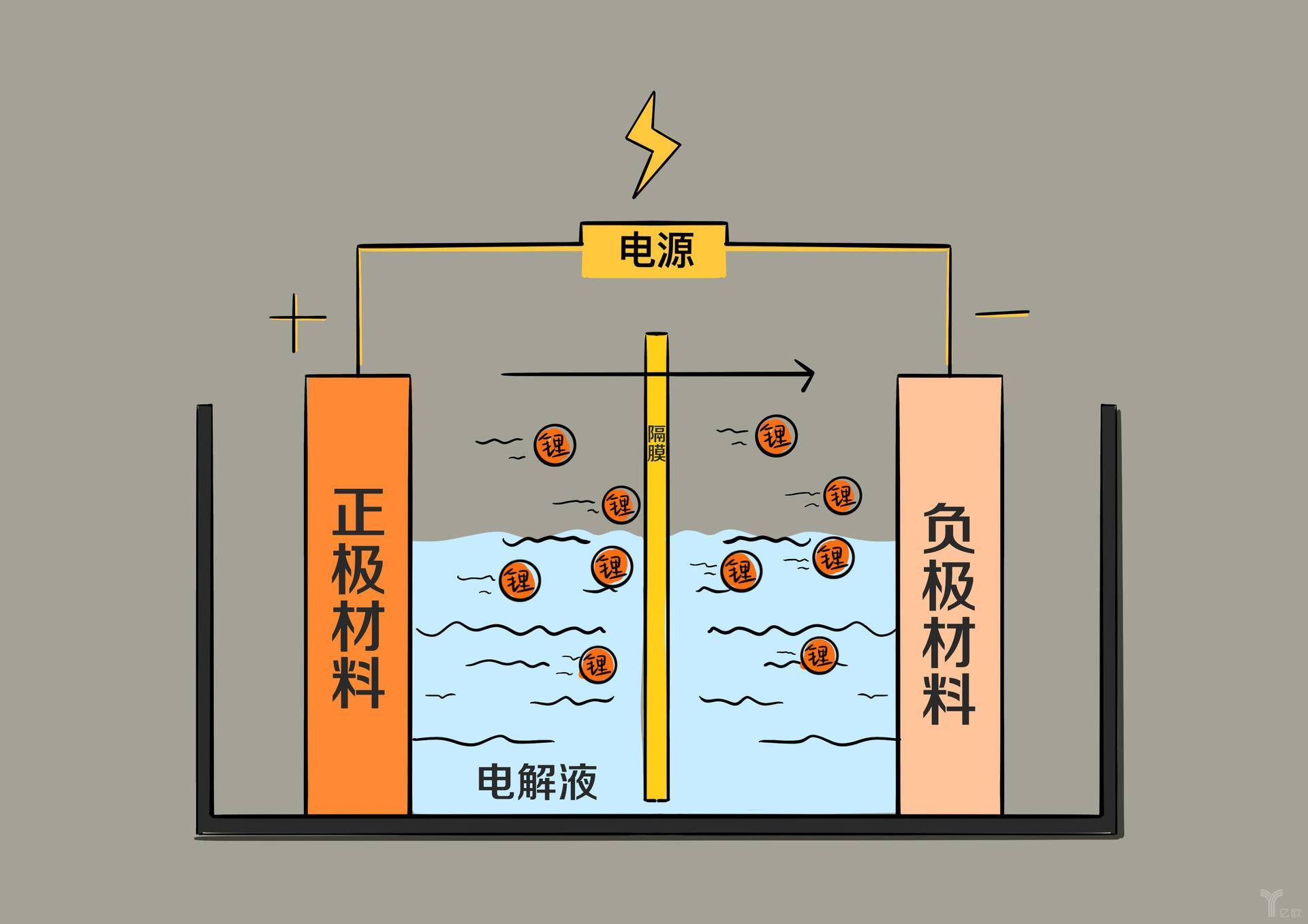
锂殿崇充电过程
充电则是锂离子从正极流到负极的过程,锂离子嵌入到负极。快充则是加大电流,等于是用更大的功率推进锂离子向负极加速流动。过充锂离子则会堆积在负极,锂离子堆积的越多就会形成“锂枝晶”。而锂电池的爆炸或者起火,基本都是因为锂枝晶生长太长了,刺穿了隔膜导致锂电池内部短路。电池内部因短路造成温度急剧上升,就会起火爆炸。
过充:锂离子形成锂枝晶:

锂离子堆积形成锂枝晶
小结:越是实名的锂电池企业,对于质量的把控越严格,从各种技术手段来减少锂电池的危险性。不管从极板、隔膜、电解液等材料的选择上,还有电池各种参数的把控,都具有一套或多套成熟的方案,用以解决锂电池安全性。所以大家购买锂电池或者改装锂电池一定要选择大品牌的正品电池。一定杜绝小作坊生产的锂电池,小作坊不具备技术实力,一旦选择会对我们的安全造成极大的威胁!
